En este caso, no hay que considerar los electrones ubicados en átomos o iones individuales como se indicaba en el formalismo del campo cristalino, sino en órbitas multicéntricas. Pero el color resultante se debe igualmente a los distintos niveles de energía que tienen dichas órbitas y a las probabilidades de transición electrónica que ocurren entre ellas.
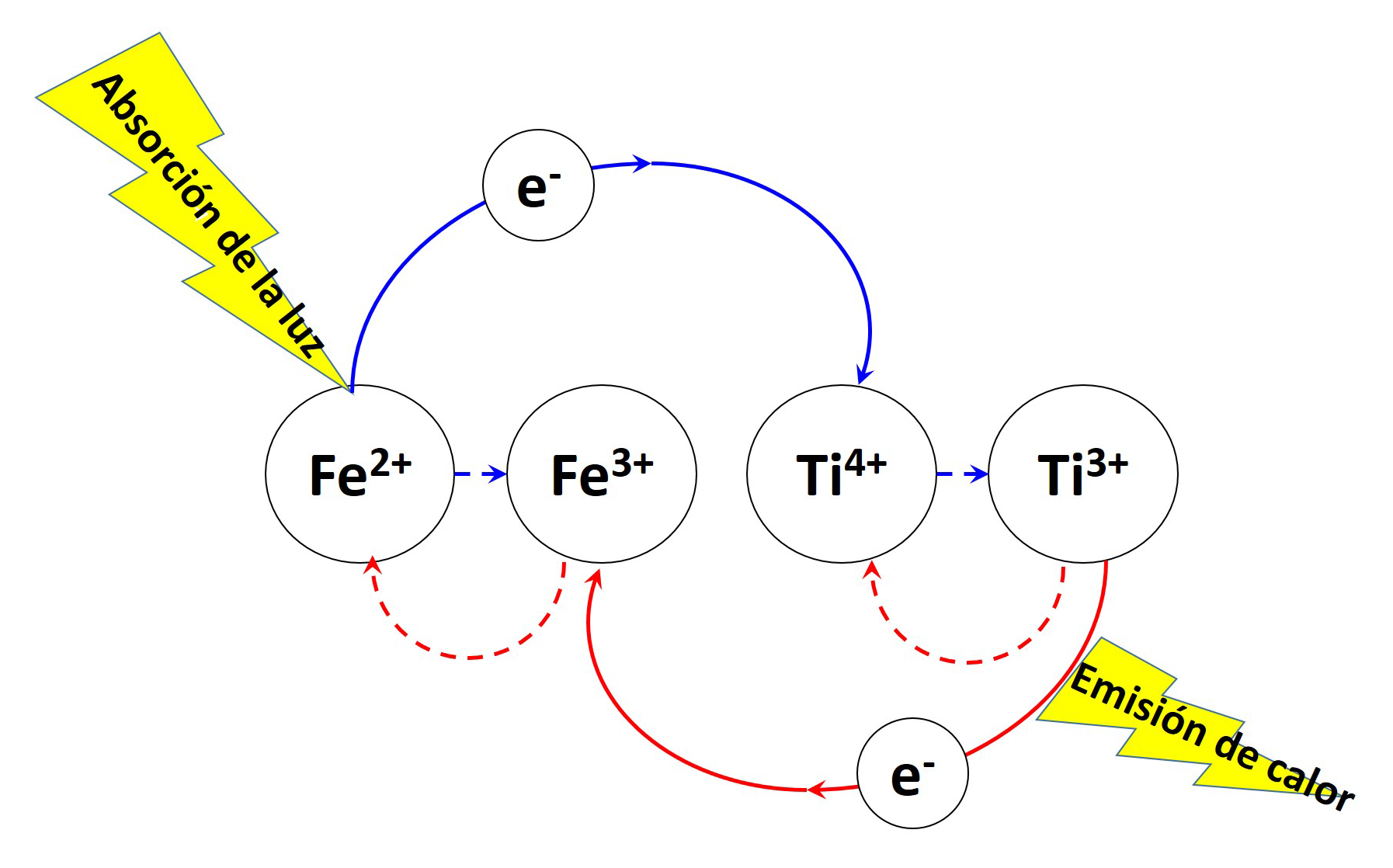
Por ejemplo, pueden existir elementos en diferentes estados de valencia que se enlacen de forma covalente y algunos electrones en las capas externas pueden viajar entre ambos iones. Esto da como resultado una transferencia de carga entre los dos iones y sólo puede ocurrir a través de la absorción de energía. Cuando la energía requerida para esa transición es equivalente a la energía en el rango de la luz visible, resultará en color.
Los resultados varían según se trate de transferencias electrónicas entre metal-metal, metal-no metal o no metal-no metal. En los dos últimos casos el tipo de enlace suele ser predominantemente covalente.